
|
|
ENSIKLOPEDIA ELEKTRONIK RADIO DAN KEJURUTERAAN ELEKTRIK Ciri-ciri perbandingan sel galvanik bersaiz AA. Ensiklopedia elektronik radio dan kejuruteraan elektrik
Ensiklopedia elektronik radio dan kejuruteraan elektrik / Pengecas, bateri, sel galvanik Hari ini anda boleh menemui banyak unsur galvanik yang berbeza di kedai dan pasaran. Mana satu nak pilih? Artikel ini akan membantu anda membuat keputusan yang betul. Sel galvanik dan bateri digunakan secara meluas untuk menggerakkan pelbagai peralatan elektronik. Elemen yang paling biasa ialah saiz AA. Di rak jualan anda boleh menemui produk serupa daripada syarikat yang berbeza, terutamanya daripada dua sistem elektrokimia: salin dan alkali. Baru-baru ini, Energizer mula menghasilkan sel litium bersaiz AA 1,5 V. Ciri yang paling penting bagi sel galvanik - kapasiti (jumlah elektrik yang mampu dihantar ke beban) - hampir tidak pernah ditunjukkan pada label. Pembeli hanya boleh bergantung pada iklan televisyen tentang sel yang "bertahan sehingga sepuluh kali lebih lama daripada sel garam konvensional," atau mengambil kata Energizer bahawa sel litium e2 bersaiz AA baharunya bertahan lima kali lebih lama daripada sel alkali konvensional [1]. Lebih-lebih lagi, masih belum jelas sepenuhnya elemen mana yang dipanggil "biasa". Untuk membandingkan secara kuantitatif parameter unsur sistem elektrokimia yang berbeza, adalah perlu untuk mengujinya di bawah keadaan yang sama. Ujian sedemikian telah dijalankan dengan tiga jenis elemen: garam Philips Long Life (EMF unsur "segar" - 1,65 V), Duracell Ultra MZ (1,62 V) alkali dan lithium Energizer e2 (1,8 V). Setiap daripada mereka dimuatkan dengan perintang 15 ohm, yang sepadan dengan arus nyahcas awal kira-kira 100 mA. Untuk elemen saiz standard AA, arus beban ini adalah tipikal. Pelepasan telah dijalankan dalam kitaran beberapa jam sehari, yang sepadan dengan keadaan operasi sebenar. Ini menerangkan voltan "pancang" pada lengkung nyahcas yang ditunjukkan dalam Rajah. 1. Lengkung biru sepadan dengan unsur garam, merah dengan unsur alkali dan hijau dengan unsur litium. Semasa tempoh "rehat", voltan pada elemen apa-apa jenis meningkat sedikit, tetapi selepas menyambungkan beban, ia dengan cepat menurun kepada minimum dalam kitaran sebelumnya. Titik menandakan nilai EMF unsur - voltan padanya tanpa beban.
Jika kita mengambil sebagai kriteria untuk nyahcas lengkap sel penurunan voltan pada bebannya kepada 0,9 V, kapasiti sel garam yang ditentukan secara eksperimen ialah 1 Ah, sel alkali ialah 2,9 Ah, dan sel litium ialah 3,5 Ah. . Akibatnya, tidak perlu bercakap tentang apa-apa perbezaan lima dan sepuluh kali ganda dalam kapasiti unsur sistem elektrokimia yang berbeza. Dalam Rajah. Rajah 2 menunjukkan satu lagi siri lengkung.
Mereka menunjukkan bagaimana rintangan dalaman unsur-unsur berubah semasa proses pelepasan. Korespondensi antara jenis elemen dan warna lengkung di sini adalah sama seperti dalam Rajah. 1. Nilai rintangan dalaman R dikira menggunakan formula
di mana E ialah EMF unsur; U - voltan di bawah beban; RH - rintangan beban. Rintangan dalaman unsur-unsur garam dan alkali meningkat secara monoton apabila pelepasan berlangsung. Dan rintangan litium, setelah menurun secara mendadak pada permulaan pelepasan, kekal praktikal tidak berubah sehingga akhir, dan kemudian meningkat dengan mendadak. Sudah tentu, eksperimen yang dijalankan tidak boleh dipanggil menyeluruh. Kapasiti sesuatu elemen bukanlah nilai tetap; ia bergantung kepada banyak faktor luaran. Untuk elemen yang berbeza, maksimumnya boleh dicapai dalam keadaan pelepasan yang berbeza dengan ketara. Untuk mengambil kira semua ini, adalah perlu untuk menjalankan satu siri eksperimen yang sangat besar, tidak realistik dalam keadaan amatur. Walau bagaimanapun, mari kita cuba menyemak keputusan yang diperolehi dengan pengiraan. Untuk menganggarkan kapasiti maksimum yang mungkin secara teori bagi unsur-unsur pelbagai sistem elektrokimia, anda perlu mengetahui komposisi kimia elektrodnya, elektrolit dan tindak balas kimia yang berlaku dalam unsur tersebut. Untuk sel garam dan alkali, katod adalah zink dan anod adalah mangan dioksida. Atas sebab inilah unsur-unsur tersebut secara kolektif dipanggil mangan-zink. Tetapi elektrolit di dalamnya berbeza: garam (biasanya ammonium klorida) atau alkali (kalium hidroksida). Menurut [2], tindak balas berlaku dalam unsur garam mangan-zink
dan dalam alkali
Tiada maklumat yang boleh dipercayai tentang bahan elektrod dan tindak balas kimia dalam sel litium. Seseorang hanya boleh menganggap bahawa elektrod adalah litium dan mangan dioksida, dan elektrolit adalah larutan litium perklorat dalam propilena karbonat. Jika tekaan ini betul, menurut [2], tindak balas berlaku dalam sel litium
Dengan menggunakan hukum Faraday, kita memperoleh ungkapan untuk menentukan kapasiti sel galvanik C, Ah:
di mana m ialah jisim bahan bertindak balas F = 96,5-103 C/g-eq - Nombor Faraday; n - valens (untuk garam dan sel galvanik alkali - 2, untuk litium - 1); M ialah jumlah berat molekul bahan bertindak balas. Kami menimbang sel galvanik saiz AA: garam - 17 g, beralkali - 24 g, litium - 15 g. Mari kita anggap bahawa, berbanding dengan jisim bahan bertindak balas, jisim badan sel dan bahan yang tidak mengambil bahagian. dalam tindak balas (elektrod karbon, elektrolit dalam sel alkali dan litium ), boleh diabaikan dan boleh diabaikan. Kami mengira jumlah berat molekul bahan bertindak balas daripada persamaan tindak balas kimia di atas: untuk garam - 346 g, untuk alkali - 257 g, untuk litium - 94 g. Menggantikan nilai berangka ke dalam formula, kami memperoleh maksimum yang mungkin. kapasiti sel garam - 2,6 Ah , alkali - 5 Ah, litium - 4,3 Ah. Perbezaan antara nilai kapasitansi yang dikira dan yang diukur boleh dijelaskan oleh andaian yang agak kasar yang dibuat dalam pengiraan. Jadi tiada perbezaan lima atau sepuluh kali ganda ditemui. Kapasiti teori sel alkali adalah lebih kurang dua kali ganda berbanding sel garam, dan litium tidak mempunyai kelebihan berbanding alkali dalam hal ini. Ini konsisten dengan keputusan eksperimen. Berdasarkan hasil semua kerja yang dilakukan, kita boleh menyimpulkan perkara berikut: 1. Sel galvanik litium mempunyai voltan yang paling stabil, rintangan dalaman yang paling rendah, yang boleh dikatakan tidak bergantung pada tahap pelepasan, dan kapasiti tertinggi, walaupun tidak banyak. Ia lebih baik digunakan untuk peralatan kuasa dengan penggunaan arus tinggi, serta dalam peranti yang dimatikan secara automatik apabila voltan bekalan kuasa menurun (contohnya, kamera digital). 2. Sel alkali mempunyai kapasiti yang setanding dengan litium dan juga mampu menghantar arus tinggi ke beban, tetapi pada voltan yang lebih rendah. Mereka paling baik digunakan dalam peranti dengan penggunaan arus purata tanpa kawalan voltan automatik. Dalam banyak kes, sel alkali lebih disukai berbanding sel litium kerana ia adalah tiga hingga empat kali lebih murah. 3. Sel garam mempunyai kapasiti terkecil dan rintangan dalaman yang paling tinggi. Adalah dinasihatkan untuk menggunakannya dalam peralatan dengan penggunaan arus yang rendah. Kesusasteraan
Pengarang: I.Podushkin, Moscow
Perangkap udara untuk serangga
01.05.2024 Ancaman serpihan angkasa kepada medan magnet Bumi
01.05.2024 Pemejalan bahan pukal
30.04.2024
▪ LG akan melancarkan telefon dengan paparan OLED yang fleksibel ▪ Superkomputer mudah alih untuk kenderaan tanpa pemandu ▪ Navigator di cermin depan kereta ▪ Basikal Gunung Elektrik Vitus E-Mythique LT
▪ bahagian tapak Penstabil voltan. Pemilihan artikel ▪ artikel oleh François Fénelon. Kata-kata mutiara yang terkenal ▪ Bagaimanakah jam matahari memberitahu masa? Jawapan terperinci ▪ artikel Herotan terma dalam penguat HiFi. Ensiklopedia elektronik radio dan kejuruteraan elektrik ▪ Sesi Artikel dengan cecair (beberapa helah). Fokus Rahsia
Komen pada artikel: tetamu Artikel yang bagus, terima kasih.
Laman utama | Perpustakaan | artikel | Peta Laman | Ulasan laman web www.diagram.com.ua |






 Arabic
Arabic Bengali
Bengali Chinese
Chinese English
English French
French German
German Hebrew
Hebrew Hindi
Hindi Italian
Italian Japanese
Japanese Korean
Korean Malay
Malay Polish
Polish Portuguese
Portuguese Spanish
Spanish Turkish
Turkish Ukrainian
Ukrainian Vietnamese
Vietnamese






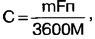
 Tinggalkan komen anda pada artikel ini:
Tinggalkan komen anda pada artikel ini: